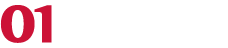Per la stampa di ossa anche gli scienziati dell'Università di Bristol hanno sviluppato un bio-inchiostro contenente cellule staminali, con il quale alimentare una classica stampante 3D alimentata in retrofit con un liquido che diventa gel a 37°C.
Si tratta d'un procedimento sperimentale sempre più affermato, che in questo caso è stato specializzato sulle ossa.
Questo bio-inchiostro contiene due differenti componenti polimerici: un polimero naturale estratto da alghe, coadiuvato da un secondo polimero, di tipo sintetico, molto usato nel settore medico.
Aumentando la temperatura, il polimero sintetico provoca il cambio di stato del bio-inchiostro da liquido a solido, e il derivato delle alghe fornisce supporto strutturale quando vengono introdotti i nutrienti cellulari.
«Serve un materiale stampabile, abbastanza forte per mantenere la sua forma quando immerso in sostanze nutritive e che non è dannoso per le cellule», ha dichiarato Adam Perriman, uno dei ricercatori che hanno sviluppato il procedimento; «ci siamo riusciti, ma dopo molti tentativi».
Il procedimento studiato a Bristol è proseguito nel differenziare le cellule staminali in osteoblasti e condrociti.
Gli osteoblasti sono cellule che secernono la sostanza che crea le ossa, mentre i condrociti creano la matrice della cartilagine. Il procedimento ha generato tessuti complessi, fino ad un anello tracheale completo (che è composto di cartilagine) a dimensione reale, in un arco di cinque settimane.
La stampante da banco 3D retrofit viene alimentata da un composto liquido che a 37° diventa un gel. In questo modo è possibile sviluppare complesse architetture biologiche.
Successivi sviluppi potrebbero portare alla stampa di tessuti complessi utilizzando le cellule staminali del paziente per chirurgia ossea o impianti cartilaginei del ginocchio e dell'anca.
I risultati sono descritti in "3D Bioprinting using a templated porous bioink" da James P. K. Armstrong, Madeline Burke, Benjamin M. Carter, Sean A. Davis e Adam W. Perriman, e pubblicati in Advanced Healthcare Materials.
“Introducendo i nutrienti delle cellule, il polimero sintetico viene completamente espulso dalla struttura 3D, lasciando solo le staminali e il polimero ottenuto dalle alghe”, ha continuato Perriman; “ciò crea pori microscopici, essenziali per l'accesso di nutrienti per le cellule staminali”.